Phản Ứng Giữa Khí Carbon Dioxide (CO2) và Dung Dịch Calcium Hydroxide (Ca(OH)2)

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Phản ứng hóa học giữa khí carbon dioxide (CO2) và dung dịch calcium hydroxide (Ca(OH)2), thường được biết đến với tên gọi nước vôi trong, là một trong những phản ứng kinh điển và quan trọng trong hóa học, đặc biệt được sử dụng rộng rãi để nhận biết sự có mặt của khí CO2.
Carbon dioxide (CO2) là một khí không màu, không mùi, nặng hơn không khí, được tạo ra từ quá trình hô hấp, đốt cháy nhiên liệu hóa thạch và các quá trình công nghiệp. Calcium hydroxide (Ca(OH)2) là một bazơ mạnh, ít tan trong nước, tạo thành dung dịch trong suốt gọi là nước vôi trong.
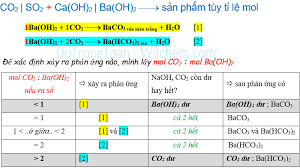
Giai đoạn 1: Sủi khí CO2 vào dung dịch Ca(OH)2 vừa đủ
Khi khí CO2 được sục vào dung dịch nước vôi trong (Ca(OH)2), phản ứng hóa học xảy ra ngay lập tức. Sản phẩm chính của phản ứng này là calcium carbonate (CaCO3) và nước (H2O). Calcium carbonate là một chất rắn màu trắng, không tan trong nước, chính là thành phần chính của đá vôi, vỏ trứng, và ngọc trai.
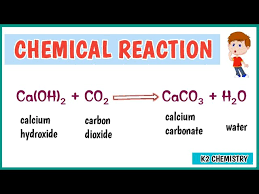
Phương trình hóa học cho phản ứng này như sau:
CO2(khí) + Ca(OH)2(dd) → CaCO3(rắn)↓ + H2O(lỏng)
Hiện tượng quan sát được: Dung dịch nước vôi trong ban đầu trong suốt sẽ trở nên vẩn đục, sau đó xuất hiện kết tủa trắng đục. Điều này là do sự hình thành của calcium carbonate rắn, không tan, lơ lửng trong dung dịch. Phản ứng này được sử dụng làm "phép thử nước vôi trong" để nhận biết CO2: nếu sục một khí vào nước vôi trong mà tạo kết tủa trắng, khí đó có khả năng cao là CO2.
Giai đoạn 2: Sủi khí CO2 dư vào dung dịch chứa kết tủa CaCO3
Nếu tiếp tục sục khí CO2 vào dung dịch đã có kết tủa CaCO3, một phản ứng hóa học khác sẽ xảy ra. Calcium carbonate (CaCO3) lúc này sẽ phản ứng với lượng CO2 dư và nước để tạo thành calcium bicarbonate (Ca(HCO3)2).
Phương trình hóa học cho phản ứng này như sau:
CaCO3(rắn) + CO2(khí) + H2O(lỏng) → Ca(HCO3)2(dd)
Hiện tượng quan sát được: Kết tủa trắng đục của calcium carbonate sẽ dần tan biến, làm cho dung dịch trở nên trong suốt trở lại. Điều này là do calcium bicarbonate (Ca(HCO3)2) là một hợp chất tan được trong nước.
Calcium bicarbonate là nguyên nhân chính gây ra "độ cứng tạm thời" của nước. Khi nước cứng tạm thời được đun sôi, calcium bicarbonate sẽ phân hủy trở lại thành calcium carbonate, gây ra hiện tượng cặn trắng bám vào ấm đun nước hoặc đường ống.
Ứng dụng và ý nghĩa của phản ứng:
- Nhận biết CO2: Là phương pháp thử kinh điển và đơn giản nhất để xác định sự có mặt của khí CO2.
- Công nghiệp: Được sử dụng trong quá trình sản xuất soda (quy trình Solvay), xử lý nước thải để loại bỏ CO2 hoặc điều chỉnh pH, và trong sản xuất vật liệu xây dựng.
- Sinh học và Địa chất: Phản ứng này giải thích sự hình thành và tan rã của các hang động đá vôi (do CO2 trong nước mưa hòa tan đá vôi tạo thành các hang động) và sự hình thành cặn đá vôi trong các hệ thống nước tự nhiên.
- Độ cứng của nước: Hiểu rõ cơ chế tạo thành và loại bỏ độ cứng tạm thời trong nước.