Phenol Không Phản Ứng Với Các Chất Nào? Phân Tích Chi Tiết

Chính Sách Vận Chuyển Và Đổi Trả Hàng
Miễn phí vận chuyển mọi đơn hàng từ 500K
- Phí ship mặc trong nước 50K
- Thời gian nhận hàng 2-3 ngày trong tuần
- Giao hàng hỏa tốc trong 24h
- Hoàn trả hàng trong 30 ngày nếu không hài lòng
Mô tả sản phẩm
Phenol (C6H5OH) là một hợp chất hữu cơ quan trọng, thuộc nhóm hợp chất hydroxy thơm. Mặc dù được biết đến với khả năng phản ứng mạnh mẽ ở cả nhóm -OH và vòng benzen, phenol vẫn có những giới hạn về mặt hóa học và không phản ứng với một số loại chất nhất định trong điều kiện thông thường. Việc hiểu rõ những phản ứng không xảy ra này là rất quan trọng để nắm vững tính chất hóa học của phenol và phân biệt nó với các hợp chất khác.
Dưới đây là phân tích chi tiết về các loại chất mà phenol không phản ứng hoặc rất khó phản ứng trong điều kiện thông thường:
1. Với dung dịch muối cacbonat và bicacbonat (ví dụ: Na2CO3, NaHCO3)
Đây là một trong những điểm khác biệt quan trọng nhất giữa phenol và các axit cacboxylic. Phenol có tính axit yếu (pKa khoảng 10), yếu hơn axit cacbonic (H2CO3, pKa1 khoảng 6.35). Do đó, phenol không đủ mạnh để đẩy axit cacbonic ra khỏi muối của nó. Điều này có nghĩa là khi cho phenol vào dung dịch natri cacbonat (Na2CO3) hoặc natri bicacbonat (NaHCO3), sẽ không có phản ứng hóa học xảy ra, không có khí CO2 thoát ra. Đây là một phương pháp quan trọng để phân biệt phenol với các axit cacboxylic như axit axetic (CH3COOH) hoặc axit benzoic (C6H5COOH), vốn sẽ phản ứng mạnh với NaHCO3 tạo khí CO2.
2. Với các kim loại kém hoạt động hoặc ít hoạt động
Phenol có khả năng phản ứng với các kim loại kiềm mạnh như Na hoặc K, tạo ra phenolat và giải phóng khí H2. Tuy nhiên, tính axit của phenol không đủ mạnh để phản ứng với các kim loại kém hoạt động hơn như đồng (Cu), bạc (Ag), sắt (Fe), hoặc bạch kim (Pt) trong điều kiện thường. Ví dụ, khi nhúng một thanh đồng vào phenol lỏng hoặc dung dịch phenol, sẽ không có phản ứng nào quan sát được.
3. Với các axit vô cơ mạnh (loãng) hoặc axit hữu cơ (như một bazơ)
Phenol có nhóm -OH, nhưng oxy trong nhóm -OH này không có tính bazơ đáng kể để phản ứng với axit vô cơ mạnh (như HCl loãng, H2SO4 loãng) hoặc axit hữu cơ (như CH3COOH) để tạo thành muối. Nói cách khác, phenol không đóng vai trò là một bazơ trong các phản ứng axit-bazơ thông thường. Mặc dù vòng benzen của phenol có thể tham gia phản ứng thế electrophin với axit mạnh (như nitro hóa bằng HNO3 hoặc sulfon hóa bằng H2SO4 đậm đặc), nhưng đó không phải là phản ứng giữa nhóm -OH và axit theo kiểu axit-bazơ.
4. Với các tác nhân khử nhẹ hoặc trung bình
Nhóm hydroxyl (-OH) của phenol không dễ dàng bị khử bởi các tác nhân khử thông thường như natri borohydrua (NaBH4) hay liti nhôm hydrua (LiAlH4), vốn thường được dùng để khử nhóm cacbonyl (aldehyd, keton, axit cacboxylic) hoặc một số liên kết đôi. Để khử hoàn toàn vòng benzen của phenol thành cyclohexanol, cần các điều kiện khắc nghiệt hơn như hydro hóa xúc tác (H2/Ni, Pt hoặc Pd) ở nhiệt độ và áp suất cao.
5. Với các tác nhân oxi hóa nhẹ hoặc trung bình (trong một số trường hợp)
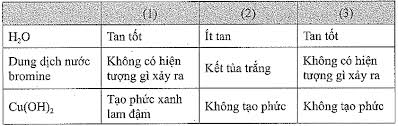
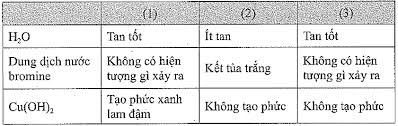
Mặc dù phenol dễ bị oxi hóa bởi các tác nhân mạnh (như KMnO4) hoặc thậm chí bởi không khí (dẫn đến sự đổi màu hồng/nâu khi để lâu), nhưng nó khá bền vững đối với một số tác nhân oxi hóa nhẹ hoặc trong điều kiện không đủ mạnh. Ví dụ, phenol thường không bị oxi hóa bởi H2O2 loãng trong điều kiện thường mà không có xúc tác. Tuy nhiên, cần lưu ý rằng phenol rất dễ bị oxi hóa ở vòng thơm, đặc biệt là với nước brom (Br2/H2O) – một phản ứng điển hình để nhận biết phenol, tạo kết tủa trắng 2,4,6-tribromophenol.
6. Với nước (chỉ hòa tan, không phản ứng hóa học)
Phenol có độ tan hạn chế trong nước (khoảng 8,3 g/100 mL ở 20°C). Khi hòa tan vào nước, nó phân li rất yếu để tạo ra ion phenolat và H3O+, thể hiện tính axit rất yếu. Tuy nhiên, không có phản ứng hóa học nào xảy ra giữa phenol và nước để tạo ra một hợp chất mới bền vững, giống như cách este phản ứng với nước để tạo axit và ancol (thủy phân) hoặc anken phản ứng với nước để tạo ancol (cộng hợp).
Kết luận:
Phenol là một hợp chất đa năng với nhiều phản ứng hóa học quan trọng, đặc biệt là tính axit và khả năng tham gia phản ứng thế electrophin trên vòng thơm. Tuy nhiên, việc nhận biết các chất mà phenol không phản ứng với chúng, đặc biệt là dung dịch muối cacbonat/bicacbonat và các kim loại kém hoạt động, là chìa khóa để hiểu rõ hơn về tính chất đặc trưng của nó và áp dụng trong các bài toán nhận biết, phân loại hợp chất hữu cơ.